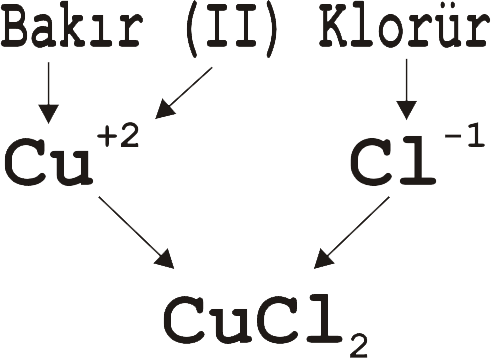|
Metal - Ametal Bileşiklerin Adlandırılması
Herhangi bir bileşik hangi atomlar veya atom gruplarından yapılmış olursa olsun.
Tüm bileşiklerin elektriksel olarak nötral olduğunu biliyoruz.
Bu nedenle Tablo-1 de gösterilen türler bir bileşik oluşturmak üzere bir araya gelirlerken
molekül içindeki yük dengesinin korunması gerektiğini kolayca söyleyebiliriz.
Örneğin +3 değerlikli altın iyonunun -1 değerlikli Br iyonuyla oluşturacağı bileşiğin forümlünün nasıl yazılacağını
ve yazılan formülün nasıl adlandırılacağını görelim.
|
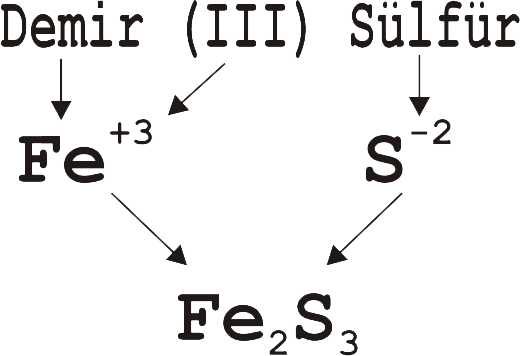
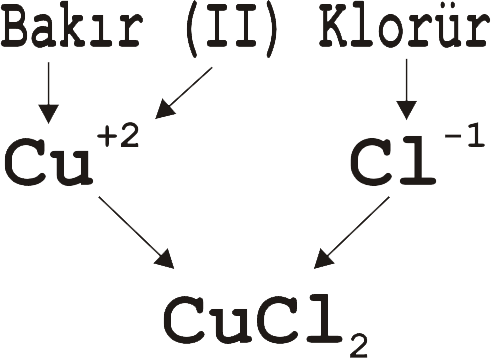
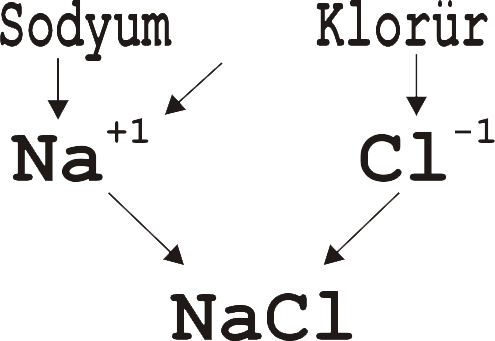
Sodyum bileşiklerinde yalnızca +1 değeri aldığından
sodyum (I) klorür diye adlandırmıyoruz.
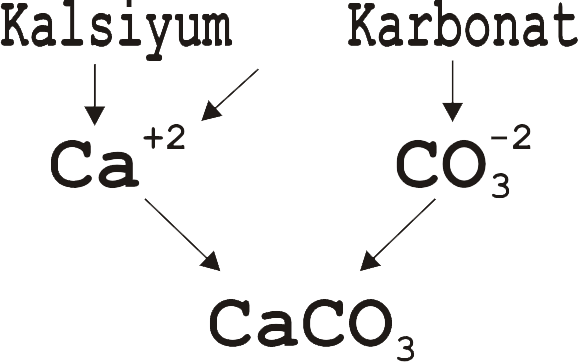
Kalsiyum yalnızca +2 değer aldığından kalsiyum (II) karbonat olarak isimlendirilmez.
Bir kalsiyum iyonu bir karbonat iyonu ile nötral bileşik oluşturduğundan
kalsiyum karbonat formülü
Ca2(CO3)2
şeklinde yazılmaz.
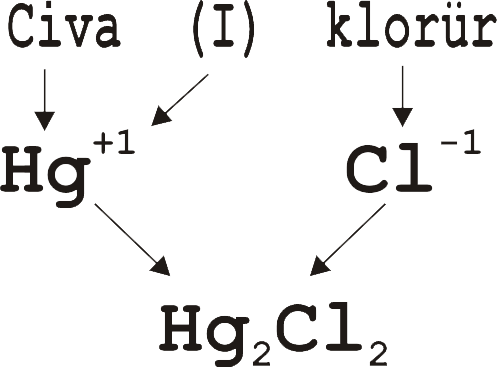
Yukarıda öğrendiklerimiz ve yandaki örnekler doğrultusunda
Civa (I) klorür bileşiğinin formülünü HgCl
şeklinde yazmamız gerektiğini düşünürüz.
Bazen bu yazım desenine rastlansada doğrusu bu değildir.
Çünkü bileşik içerisinde civanın bir değerli olarak düşündüğümüz iyonu
Hg2+2 şeklinde bulunur.
Bu nedenle bileşğin doğru yazımı HgCl değil Hg2Cl2 dir.
|
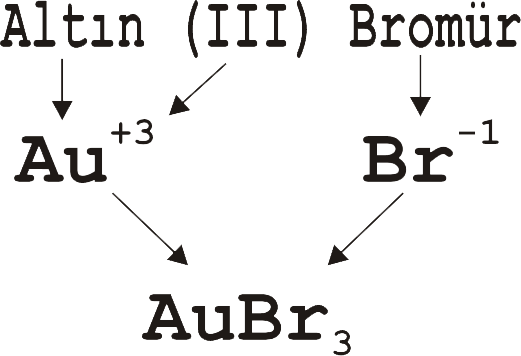
Tablo 1 den altının bileşik içerisinde Au+3 şeklinde +3 değerli olarak bulunabileceği verilmiştir.
Brom ise Br- ise şeklinde -1 değerli olarak bulunabileceği görülmektedir.
Bu iki tür bir araya gelerek bir bileşik oluşturacaksa elektriksel nötralliğin sağlanması için 1 Au+3 karşılık 3 Br- bileşik içinde yer alması gerekir.
Kimyasal formülleri yazmak için;
Pozitif yüklü atomun sembolü yazılır. Molekül içindeki atom sayısı (daha doğrusu iyon sayısı) indis olarak belirtilir. İstisnai durum olarak eğer molekül içindeki atom sayısı 1 tane ise indis olarak yazılmaz. İkinci bileşiğin sembolü yazılır. Molekül içindeki atom sayısı (daha doğrusu iyon sayısı) indis olarak belirtilir. İstisnai durum olarak eğer molekül içindeki atom sayısı 1 tane ise indis olarak yazılmaz.
Kimyasal formülü adlandırmak için;
Pozitif yüklü atomun adı yazılır. Değerliği romen rakamı ile parantez içinde belirtilir. Eğer atom bileşiklerinde tek değer alıyorsa belirtmeye gerek yoktur. Negatif yüklü türün adı söylenir ve sonuna -ür, -it vaya -at takısı getirilir.
|
Ametal - Ametal Bileşiklerin Adlandırılması
Yukarıdaki isimlendirmelerde bir metal iyonu ve bir anyon arasında meydana gelen isimlendirmeleri kapsar.
Fakat pekçok bileşikte bir metal iyonu ile bir anyon arasında meydana gelmez.
Bu durumda ametal-ametal isimlendirilmesinin kullanılması gerekir.
Bu adlandırma metal ametal adlandırmasına benzer yönleri bulunsistematiği ise yukarıdakinden farklıdır.
Örneğin HBr bileşiği metal - ametal bileşiklerinde olduğu gibi +1 değerlikli hidrojen önce -1 değerlikli brom sonra yazılır ve hidrojen bromür olarak adlandırılır.
Bu kategorideki bazı bileşiklerin özel adları bulunur. Yazım deseninde de HBr için belirtilen kural uygulanmaz.
Örneğin +1 değerlikli hidrojen ile -3 değerlikli azotun bileşiği NH3 şeklinde yazılır. Geleneksel adı da amonyaktır.
Bazı ameteller kendi aralarında birden farklı sayıda bileşik yaparlar.
Bu bileşiklerin adlandırılmasında moleküldeki atomların sayılarına bağlı olarak ön ekler kullanılır.
Molekülde aynı ametalden 1 tane atom varsa mono-, 1 tane atom varsa di-,
3 tane atom varsa tri-, 4 tane atom varsa tetra-, 5 tane atom varsa penta-, 6 tane atom varsa hekza-, 7 tane atom varsa hepta-
8 tane atom varsa okta- v.b. ön ekleri elementin adının önüne getirilir. Örneğin;
N2O5 bileşiği diazot pentaoksit olarak adlandırılır.
Aşağıda bazı ametal-ametal adlandırma örnekleri verilmiştir.
|
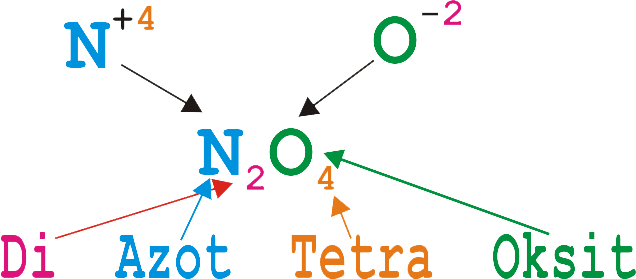
diazot tetraoksit
|
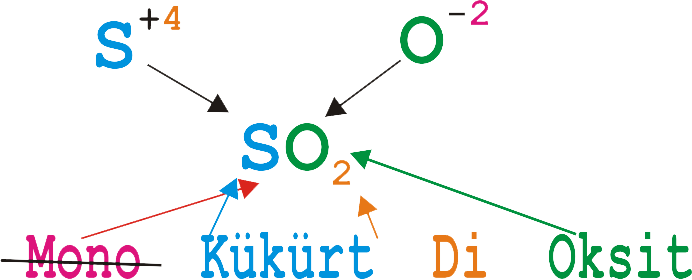
kükürt dioksit
Not: Birinci elementten molekül içerisinde
1 tane bulunduğundan onu
mono diye tanımlamaya gerek yoktur.
|
| |
|
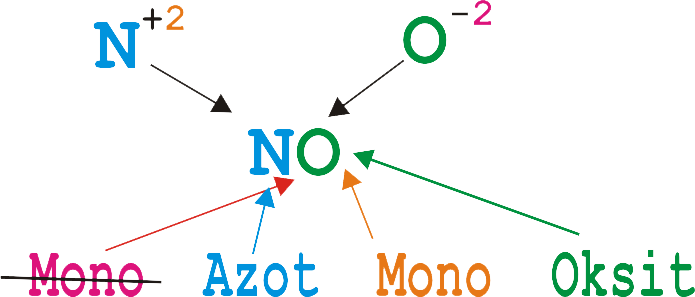
azot monoksit
|
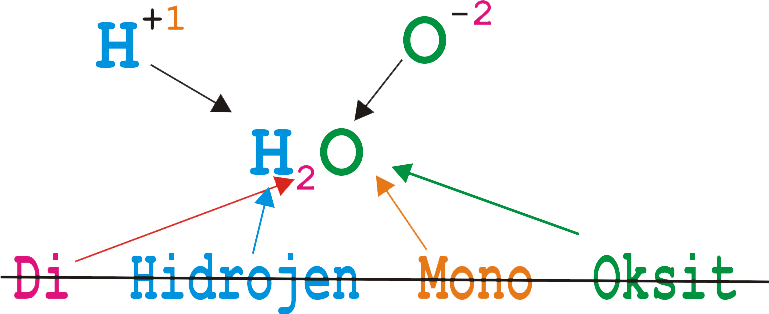
Su
Not : Bazı bileşiklerin özel isimleri vardır.
İçtiğimiz suyu isimlendirirsek
dihidrojenmonoksit adını vermemiz gerekir.
Fakat geneneksel isim su olarak kullanırız.
|
Konu İle İlgili Etkileşimli Sorular :
Metal-Ametal adlandırılması
Ametal-Ametal adlandırılması
|