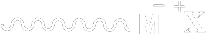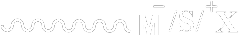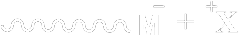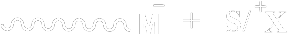Ýyonik Zincir (Katýlma) Polimerizasyonu
Bu tür polimerizasyonda çifte bađýn etrafýndaki sübstitüe gruplarýn etkisi ile yüklü bir yapý oluţur.
Zincir polimerizasyasyonu radikalik, anyonik veya katyonik olarak gerçekleţebilir.
Serbest radikal polimerizasyonunun seçiciliđi yoktur. Ancak iyonik polimerizasyon seçimlidir.
Polimerizasyon sýrasýnda Ýyonik reaksiyonlar elektrostatik kuvvetlerden etkilenir ve bu tip reaksiyonlarda reaksiyon hýzý, ortamýn polaritesi, iyon çifti yakýnlýđý ve iyonik solvatasyonuyla deđiţir. Ýyonik polimerizasyonda büyüme iyon çiftinin bulunduđu yerden olur ve iyon çiftlerinin yüksek dielektrik sabitli bir ortamda çözünmesiyle ya da çözgende ayrýlmalarý ile reaksiyon hýzý artar. Monomerle güçlü etkileţmeler söz konusuysa ürünün steroregülaritesi artar. Ýyonik polimerizasyonda anyonik sistemlerdeki denge durumlarý dört farklý ţekilde olabilir.
Katyonik polimerizasyon sistemlerinde ayný eţitliklerle gösterilebilir fakat iyonlarýn iţaretleri buradakilerin tersidir. Anyonik polimerizasyonda çözgen-reaktif iyon etkileţmeleri oldukça önemlidir. Eđer iyonlar çözgenle solvatize edilmezlerse iyonlarýn dayanýklýđý düţük olacađýndan reaksiyonlar gerçekleţmezler. Bunun yanýsýra iyonlarý iyi solvatize edebilecek su, alkol ve ketonlar gibi polar çözgenler de iyonik katalizörlerle tepkime verebilirler. Bu nedenle bu tip polimerizasyon yukarýdaki maddelere göre polariteleri daha düţük olan alkil halojenür, nitrobenzen gibi çözgenlerde gerçekleţtirilir. Bu tip çözgenlerde de iyon çifti oluţumu söz konusu olup çözgenin polaritesine ve dolayýsýyla solvatize edebilme gücüne göre oluţan iyon çifti arasýndaki uzaklýk önem kazanýr. Hatta iyon çifti oluţumunun ötesinde birbirine oldukça bađlý iyon çiftleri söz konusudur. Bu tip reaksiyonlarda sonlanma aţamasý büyüyen zincirlerin moleküler reaksiyonu ya da monomer veya çözücüye transfer ile gerçekleţir. Bu tip reaksiyonlar genellikle metal amidler, metal alkiller, elektron transferi ile baţlatýlýrlar. Çođalma aţamasý monomer tükeninceye kadar sürer ve örneđin çözeltiden polimerik anyona pozitif yüklü bir iyon transfer olmadýđýndan, polimerik anyonlar sonlanmadan kalýr. Bu nedenle polimerizasyon tamamlandýktan sonra ortama monomer ilave edilirse polimerleţme devam eder. Bu sistemlerde sonlanma reaksiyonu bulunmadýđýndan polimerizasyon reaksiyonunun hýzý genellikle çođalma reaksiyonunun hýzýna eţit kabul edilir.
Olefinlerin Anyonik Polimerizasyonu : Anyonik polimerizasyon için iki genel baţlama mekanizmasý önerilmiţtir. Ýlkinde bir bazýn monomere katýlmasýyla karbanyon oluţur. Zincir polimerizasyonu bu karbanyon üzerinden yürür.
ikincisinde ise; aktif elektron verici bir molekülün bir elektron monomerin çifte bađýna transfer edilerek bir anyon radikal oluţur. radikallerin birleţmesiyle bir dianyon oluţur. Reaksiyon bu dianyon zincir taţýyýcýsý ile yürür. Elektron transferi ile gerçekleţtirilen polimerizasyon adýný alýr.
Reaksiyonun hem anyonik hemde radikalik mekanizmayla gerçekleţebileceđi ileri sürülürsede reaksiyonun anyonik taraftan yürüdüđü belirlenmiţtir.
Metal Amidlerle Baţlatýlan Polimerizasyonlar Baţlama Aţamasý : \rm NH_3 çözücüsünde \rm KNH_2 aţađýdaki denklem göre iyonlaţýr. 
reaksiyon sonucu ortaya çýkan \rm ^- :NH_2 iyonu, monomer ile reaksiyona girerek polimerizasyonu ilerletecek türü ortaya çýkartýr. 
\rm KNH_2 için iyonlaţma dengesi ţeklinde yazýlýr. \rm K= { [NH_2^-] [K^+] \over [KNH_2]}
reaksiyonun baţlama hýzý, hýz denklemi için; \rm r_i =[NH_2^-][M]
\rm r_i = k_i { K[KNH_2] \over [K^+]} [M]
ţeklindedir. Çođalma Aţamasý : Polimerizasyonun ilerlemesinde sýrasýnda baţlama aţamasýnda oluţan iyonlar monomere 
ţeklinde katýlýr. reaksiyon ilerlemesi için hýz eţitliđi \rm r_p = k_p [M^-] [M]
olarak yazýlýr. Buradaki \rm [M^-] ; ortamdaki her tür büyüyen polimer zincirlerini gösterir. Sonlanma Aţamasý : Anyonik polimerizasyonda reaktiflerin son derece saf olmasý gerekir. Basýnç en fazla \rm 10^{-5} atm. olmalýdýr. Sonlanma tepkimesi çözücüye zincir transferi ile gerçekleţir. 
sonlanma tepkimesi için kinetik eţitlik \rm r_{ tr, NH_3 }= k_{ tr, NH_3 } [M^-][NH_3]
olacaktýr. Ayrýca \rm r_i = r_t olacađýndan; \rm k_i { K[NH_2] \over [K^+]} [M] = k_{ tr, NH_3 } [M^-][NH_3]
olacađýndan; \rm [M^-] = { k_i \over k_{ tr, NH_3 } } { [M] \over [NH_3]}
yazýlabilir. Böylece ilerleme hýzý için; \rm r_p= k_p [M^-][M] = { k_p k_i [M]^2 \over k_{ tr, NH_3 } [NH_3] }
\rm \overline{ DP }_n = { r_p\over r_i } = { k_p [M] \over k_{ tr, NH_3 } [NH_3]} = { [M] \over C_s [NH_3]}
olarak yazýlabilir. Metal alkiller, organometalik bileţikler, Grignard bileţikleri anyonik baţlatýcýlar olarak kullanýlýr. Elektron Transferi Ýle Gerçekleţtirilen Anyonik Polimerizasyonlar Elektronun monomere transferi üç ţekilde gerçekleţebilir. 1). Elektron monomere dođrudan transfer edilir. Elektronun monomere dođrudan transferi ile baţlatýcý elde edilir. 
2). Elektron önce A: gibi bir bileţiđe transferi ile kararlý çözünür bir anyon radikal kompleksin oluţmasý ve daha sonra elektronun monomere verilmesi ile anyon baţlatýcý radikal oluţur. 
3. Ýkinci durumda oluţan radikal benzeri bir radikal ile birleţerek bir dianyon oluţturur. Polimerizasyonu baţlatan bu dianyon ise polimer zincirinde son grup olarak kalýr. 
Aromatik Komplekslerle Yürütülen Anyonik Polimerizasyonlar Bu tür anyonik polimerizasyonlarda genellikle transferci madde olarak naftalin kullanýlýr. 
polimerizasyonda sonlanma aţamasý yoktur. Bunun anlamý ortamdaki monomerin tamamý polimerleţinceye kadar reaksiyon devam eder. Sonlanma aţamasý olmadýđýndan polimere canlý veya yaţayan polimerler adý verilir. Bu tür polimerler büyümekte olan anyona zincir transferi yapmayan çözücüler içerisinde gerçekleţir. Anyonik polimerizasyonun çođalma basamađý radikalik polmerizasyondan daha karmaţýktýr. \rm r_p üzerine en büyük etkiyi çözücü yapar. Bunun nedeni; anyonik polimerizasyonda anyon ile karţý anyon arasýndaki mesafenin çözücü tarafýndan belirlenmesidir. Sonlanma reaksiyonu bulunmadýđýndan sistemdeki polimerleţme hýz dođrudan çođalma reaksiyonunun hýzý olarak alýnýr. Anyonik polimerizasyon reaksiyonlarý hýzlý reaksiyonlar olduđundan kinetikleri klasik yöntemlerle takip edilemez. Bu tip hýzlý polimerizasyon reakssiyonlarýný incelemek için hýzlý akýţ yöntemi geliţtirilmiţtir. Radikalik polimerizasyonda reaksiyon hýzý \rm 10^{-7} - 10^{-9} mertebesinde iken, anyonik polimerizasyonda \rm 10^{-2} - 10^{-3} mertebesindedir. Sonlanmanýn olmadýđý bu tür polimerizasyon için polimerizasyon derecesi \rm \overline{DP}_n = { [M]\over {1 \over 2} [Katalizör]}
bađýntýsý ile verilir. Olefinlerin Katyonik Polimerizasyonu : Katyonik polimerizasyonun mekanizmasýnýn anlaţýlmasý güç olmuţtur. Friedel-Craft katalizörlerinin proton vericiliklerinin anlaţýlmasý ile katyonik polimerizasyon mekanizmasýnýn anlaţýlmasý sađlanmýţtýr. Katyonik polimerizasyonda kullanýlan baţlatýcýlar üç grupta toplanýrlar. 1). Protonlu Asitler Ýle : Asitlerin anyonu fazla nükleofilik olmamalýdýr. \rm H_2SO_4, \; HClO_4, \; Cl_3CCOOH gibi asitler protonu çifte bađlý karbonlardan birine verir ve bir karbokatyon meydana gelir. 
Bu reaksiyonlarda reaksiyon hýzý 4 etkene bađlýdýr. Bunlar; karţý iyon cinsi, iyon cinsi, çözücü ve sýcaklýktýr. Eđer anyon fazla nükleofilik özellik gösteriyorsa kovalent bađ oluţumu meydana gelir ki bu alkene asit katýlmýţ duruma karţý gelir. 2). Lewis Asitleri ile : \rm SbCl_3, AlCl_3, SnCl_4, TiCl_4 katyonik polimerizasyonda kullanýlabilir. Lewis asitleri düţük sýcaklýklarda yüksek molekül ađýrlýklý polimerik ürünlerin elde edilmesinde kullanýlýr. Ancak Lewis asitleri son derece saf olduklarý taktirde baţlatýcý olarak kullanýlamazlar. Lewis asitlerinin baţlatýcý olarak kullanýlabilmeleri için bir miktar safsýzlýk içermeleri gerekir. Bu katalizörleri aktifleţtirmek için genellikle bir miktar su, protonlu asitler, alkil halojenürleri gibi katalizörler gerekmektedir. Ancak bu katalizörler ilave edilirken optimum miktarda ilave edilmelidir. Katalizörün fazlasý ortamda transferci madde olarak etki ettiđi için yüksek molekül ađýrlýklý polimerlerin oluţmasýný engeller. \rm MX_n \; + \; RH \; \rightarrow \; H^+[MXR]^-
\rm MX_n \; + \; H_2O \; \rightarrow \; H^+[MXOH]^-
Friedel-Craft reaksiyonlarýný baţlatýlmasýnda yukarýda elde edilen ürün gerçek bir katalizör görevini görür. Katalizör-Kokatalizör kompleksinin aktifliđi bu kompleksin proton verebilme yeteneđine bađlýdýr. Örneđin; izobütilen \rm SnCl_4 katalizörü, polimerizasyonda polimerizasyon hýzýnýn kokatalizörün asitlik kuvveti arttýđý bulunmuţtur. Reaksiyonun gerçekleţtiđi çözücü de önemlidir. Aţađýdaki sýrada polimerleţme hýzý deđiţir. \rm AcOH > Nitroetan > phOH > H_2O
3). Diđer Katyon Baţlatýcýlar ile : Ýki grubun dýţýndaki baţlatýcýlar bu grupta yer alýrlar. Bunlar; \rm I_2, \; ter-butClO_4, \; (C_6H_5)_3CCl ve iyonlaţtýrýcý ýţýnlardýr ( \rm g-ýţýnlarý gibi). 
\rm \gamma -ýţýnlarý ile baţlatýlan polimerizasyonda ise; 
ţeklinde baţlatýcý tür meydana gelir. Baţlama Aţamasý Protonlu asitler, Lewis asitleri, ve diđer baţlatýcýlara göre üç mekanizma vardýr. Lewis asitleri için katalizör-kokatalizörün oluţumu ilk aţamayý oluţturur. \rm C \; + \; RH \; \rightleftharpoons \; H^+(RC)^- \qquad K = { [H^+(RC)^- ] \over [C][RH]}

Çođalma Aţamasý Ortamdaki büyüyen zincirler ile monomerlerin reaksiyonu ile gerçekleţir. 
Sonlanma Aţamasý Sonlanma aţamasýnda, katyonik zincir transfer reaksiyonlarý katyonik polimerizasyonda önemli yer tutar. Zincir transferi monomere, karţý iyona, çözücüye ve polimere yapýlabilir. Monomere Zincir Transferi Ýle : 
Burada kinetik olarak zincir sonlanmýţ olur. \rm k_{tr,M}/k_p =C_M olmak üzere; C_M polimerin mol tartýsý denetler. Karţý Ýyona Zincir Transferi Ýle : 
Büyümekte olan iyon çiftinin tekrar düzenlenmesiyle ortaya çýkar. Çözücüye Zincir Transferi Ýle : 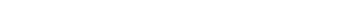
Çözücüye zincir transferi katyonik polimerizasyonlarda önemlidir. Çünkü polimerlerin alkillendirilmesi izomerleţtirilmesi veya halka oluţturmasý polimere zincir transfer reaksiyonu ile gerçekleţtirilir.
|