Gazlarýn Yođunlaţmasý, Kritik Nokta ve Karţýlýklý Haller Ýlkesi
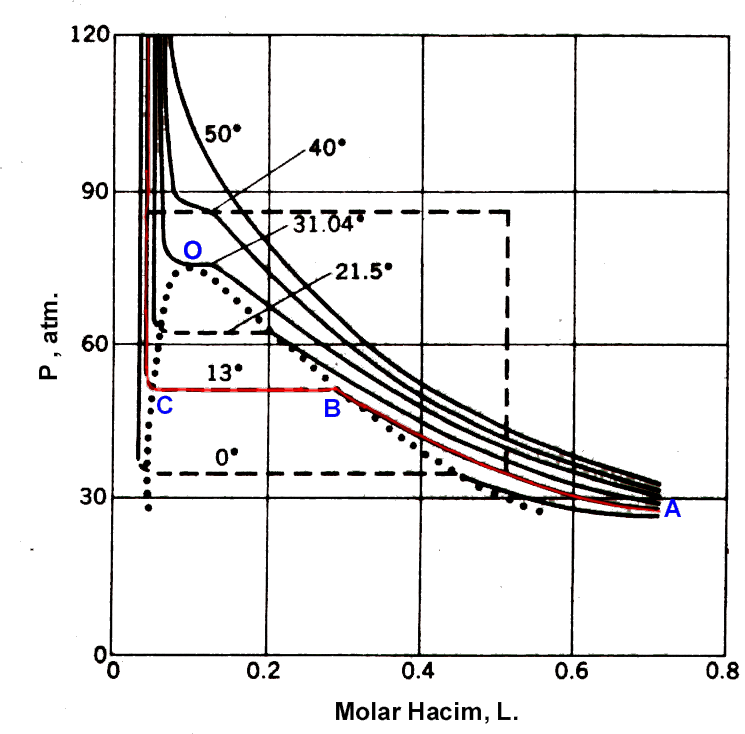
Ţekil 1 de CO2 in yođunlaţmasýný belirlemek için elde edilmiţ bir grup izotermi göstermektedir. Ţekildeki veriler gazlarýn davranýţlarý üzerine 1869 da Andrews' in çalýţmalarý sonucu elde edilmiţtir. Yüksek sýcaklýklardaki izotermler, ideal gazlar için beklenen hiperbolik eđrilerden biraz saparlarken, düţük sýcaklýk izotermlerinde ise; ideal gaz yasasýnda önemli ölçüde sapma gösterirler. Düţük basýnç deđerlerinde ideal gaz davranýţý görülür. Belli bir sýcaklýkta basýnç arttýkça hacim Boyle Yasasý'na uygun ţekilde azalýr.
Ţekildeki noktalý çizgilerle gösterilmiţ noktaya ulaţýldýktan sonra daha düţük sýcaklýklarda çalýţýlacak olursa, gazýn basýncýnýn arttýrýlmasýyla gaz sýkýţmak yerine yođunlaţýr. Ţekilde 21.5, 13 ve 0 oC de yođunlaţmanýn meydana geleceđi basýnçlar görülmektedir. Ţekilden de görüldüđü gibi karbondioksit için kritik deđer 31.04 oC dir. Bu sýcaklýđýn daha altýnda örneđin ţekildeki gibi 13 oC de A noktasýndayken basýnç arttýrýlacak olursa B noktasýna gelinceye kadar gazýn basýncý artar. Bu noktadan sonra gaz sýkýţtýrýlacak olursa basýnç deđiţmeksizin gaz sývýlaţmaya baţlar ve C noktasýna ulaţýlýr. Noktalý eđri üzerinde sývý-buhar birlikte dengededirler diđer bölgelerde yalnýzca tek tip akýţkan bulunur. Gaz sistemlerin ideal olmayan davranýţlarýna iliţkin çalýţmalardaki ilginç bir yer grafikteki noktalý çizgidir. Bu kritik izoterm olarak adlandýrýlýr. Kritik izotermin sýcaklýđý kritik sýcaklýktýr. Bu sýcaklýk sývý-buhar dengesinin bulunduđu en yüksek sýcaklýktýr. O ile gösterilmiţ olan nokta ise kritik noktadýr. Bu noktadaki basýnç, kritik basýnç ve sýcaklýk, kritik sýcaklýk olarak isimlendirilir. Bazý maddeler iliţkin kritik deđerler aţađýdaki Tablo 1 de gösterilmiţtir. 1 atm. civarýnda kuru buz ţeklindeki CO2 süblimleţir. Ţekil 2 de yüksek basýncý bir kap içinde iken sývý halde bulunan CO2 kritik sýcaklýk civarýnda gaz ve sývý arasýndaki sýnýr çizgisi kaybolarak gaz dönüţümü görülmektedir.
Gerçek gazlarýn ideallikten sapmalarý gazýn ţartlarý ve kritik nokta arasýndaki farka bađýmlýdýr. Bulunulan P,V, T deđerlerini kritik deđerlere bađlý olarak ifade edebiliriz. Bu deđerler indirgenmiţ deđiţkenler Pr, Vr ve Tr simgeleri ile \rm P_r = { P \over P_c } \; V_r = { V \over V_c } \; ve \; T_r = { T \over T_c }
eţitlikleri ile verilir. Eđer kritik deđerler bilinirse gazýn davranýţý kolayca karakterize edilebilir. Ýndirgenmiţ basýncýn bir fonksiyonu olarak Z sýkýţtýrýlabilirlik föktörü incelenebilir. Çeţitli indirgenmiţ sýcaklýklarda farklý gazlar için yapýlmýţ çalýţmalar sonucu Ţekil 2 dekine benzer grafikler elde edilir. Bu sonuçlar gazlarýn ideallikten sapmalarýnýn yalnýzca indirgenmiţ basýnç ve sýcaklýđa bađlý olduđunu gösterir. Bu ifade karţýlýklý haller ilkesini olarak adlandýrýlýr. Ýfadenin adý, ayný indirgenmiţ deđiţkenlere sahip gazlarýn ayný miktarda ideallikten sapmalarýndan hareketle verilmiţtir.
Gerçek Gazlarla Ýlgili Bertholet Denklemi Yüksek basýnçlarda Bertholet hal denklemiyle gerçek gazlarýn deneysel sonuçlarý arasýnda paralellik sađlamak mümkün deđildir. Denklem düţük basýnçlarda daha uygun deđerler vermektedir. Düţük basýnçlarda 1 mol gaz için sýkýţtýrýlabilirlik faktörü Z; \rm Z = 1 + {9 \over 128}{ P_r \over T_r} \Big( 1 - { 6 \over T_r^2} \Big)
eţitliđi ile verilir. PV=ZnRT ifadesinden hareketle ifade \rm PV=nRT \Big[ {9 \over 128}{ P_r \over T_r} \Big( 1 - { 6 \over T_r^2} \Big) \Big]
ţeklinde düzenlenebilir.
|